科技日報記者 劉霞
上個月,在美國超級碗賽事的喧囂與激情中,一則廣告悄然撥動人們的心弦:車內,一男子垂首凝望手機,屏幕上躍出一行字:“未檢測到癌癥信號”。他如釋重負,露出微笑。這則廣告的真正主角,名為Galleri——一種宣稱能于早期捕捉50多種癌癥“蛛絲馬跡”的簡易血檢技術。

Galleri只是約40種新興的多癌種早篩檢測(MCED)方法中的一員。這一方法描繪了一幅誘人圖景:它有望讓癌癥篩查更高效、更便利,也讓人們免受全身放射檢查之苦。
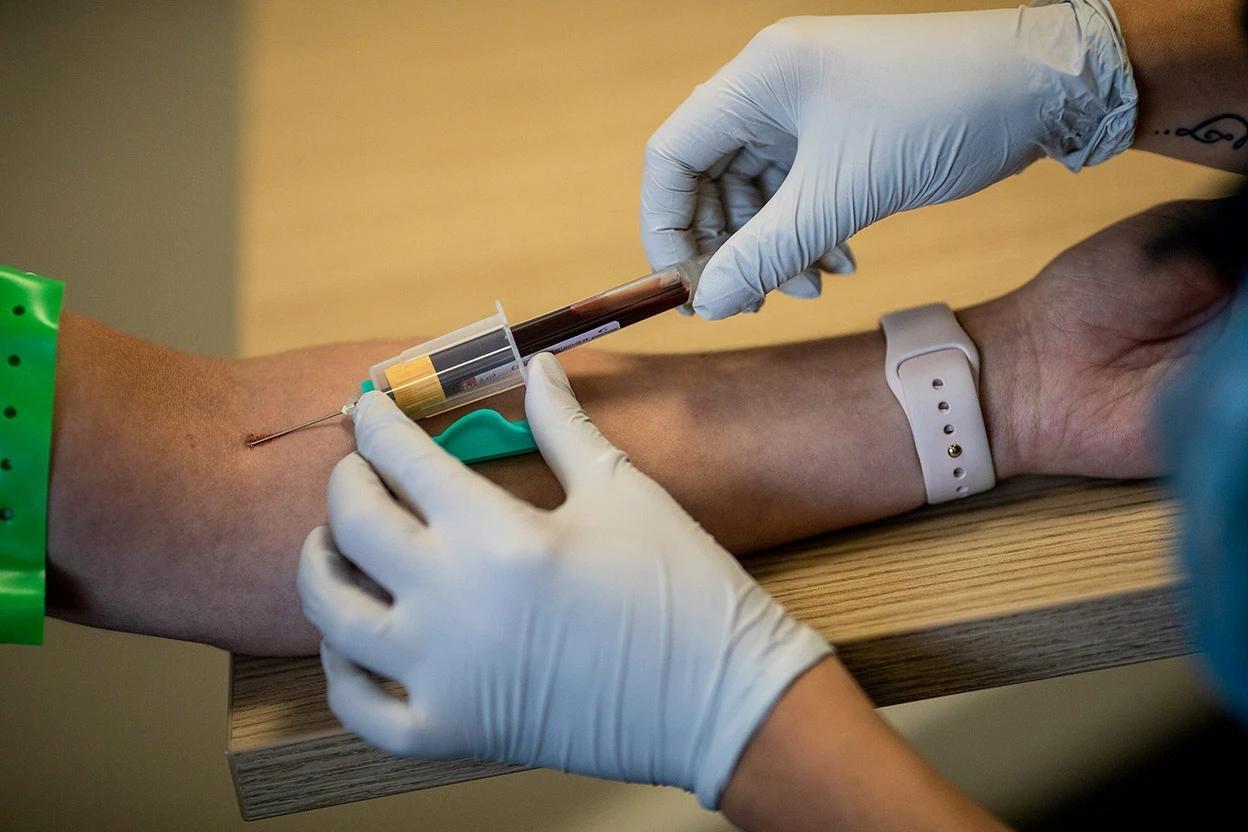
不過,《自然》網站刊文指出:盡管MCED帶來的曙光令人振奮,但其準確性與有效性,仍有待進一步考驗。
有專家認為,現有檢測仍難以發現多數早期癌癥。對普羅大眾而言,誤診的陰霾,或許會遮蔽少數人獲益的晴空。更何況,目前能通過隨機對照試驗的MCED寥寥無幾,且無一獲得監管機構的正式批準。
MCED“一專多能”
全世界約1/5的人,一生中將與癌癥“狹路相逢”。2022年,全球約970萬人因癌癥喪命。若能于癌癥萌芽階段將其“揪出”,治療創傷將更小,費用更低,患者的生存希望也更大。
英國瑪麗女王大學癌癥生物技術專家尼茨·羅森菲爾德博士表示,大多數癌癥死亡,皆因發現太晚,人們總在癥狀顯現后才去就醫。真正的解決之道,是在癥狀出現之前,便能及時發現。
這一點,正是乳腺癌、宮頸癌篩查的初衷,亦是結腸鏡檢查的目的。但這些現有篩查項目,或因檢查困難,或因覆蓋有限,遠非完美。在美國,預防性篩查僅能發現14%的確診癌癥。MCED的誘人之處,正在于其簡便且廣譜的癌癥探測潛力。
成熟的篩查技術,如乳腺X光,是“專攻一域”。而MCED則“一專多能”,可于單份血樣中,辨識出多種癌癥的生物標志物。這背后的核心理念,便是人們常說的“液體活檢”——通過一次抽血,捕捉腫瘤釋放入血液的微量信號,尤其是那些目前缺乏有效篩查手段的“隱形殺手”。
羅森菲爾認為,MCED具有潛在的革命性,若有堅實的試驗結果支撐,它們有望成為未來的護理標準。
多條路徑各顯本領
科學家早已知道,癌細胞會將自身的DNA片段釋放入血液內。此前諸多嘗試,多聚焦于尋找這些片段的基因突變。但早期階段,這些信號微乎其微,尋找它們就像“大海撈針”。例如,血液內循環腫瘤DNA(ctDNA)的占比不足0.006%。
然而,DNA測序技術進步的速度與精度,為“大海撈針”提供了可能。
2008年,美國約翰斯·霍普金斯大學的伯特·沃格爾斯坦教授證明,ctDNA可預測術后復發。2014年,沃格爾斯坦團隊開發出CancerSEEK,將ctDNA與癌癥蛋白結合分析,能識別出8種常見癌癥。該技術后來演進為能檢測50多種癌癥的Cancerguard,于去年由美國Exact科技公司推向市場。
面對血液中癌癥DNA濃度過低這一挑戰,香港中文大學盧煜明教授另辟蹊徑,從表觀遺傳變化——基因組上開啟或關閉基因的化學標記入手。其團隊開發的技術,可掃描全基因組尋找DNA甲基化標記,不僅能識別癌癥,還能定位腫瘤。這項技術被Grail公司收購,成為Galleri的基石。
此后,諸多MCED檢測技術皆基于甲基化模式。也有學者利用腫瘤DNA片段的物理特性來揭示癌癥的蛛絲馬跡。更有團隊博采眾長,如越南的SPOT-MAS,結合了遺傳突變、甲基化狀態與物理性質,用以篩查肝癌、乳腺癌、結直腸癌、胃癌和肺癌這5種常見癌癥。
數據紛紜“霧里看花”
如何評判這些檢測能否堪當大任?監管機構、醫療系統與保險公司,重點關注幾項核心指標:靈敏度(癌癥患者中檢出陽性的比例)、特異性(無癌人群中正確判為陰性的比例)以及陽性預測值(檢測陽性者中真正患癌的比例)。
系統性評估顯示,MCED的特異性高達96%—99.5%,但靈敏度僅為30%—80%。許多早期研究,僅在已知患癌者中進行,無法代表真實情景。后續的大規模人群研究,則呈現出更為復雜的圖景。
例如,一項針對無癌女性的CancerSEEK檢測,正確排除了98.9%的無癌者,但僅發現了確診的96例癌癥中的26例。Galleri的試驗結果亦相似,其特異性高達99.1%,但92名陽性者中,僅38%最終確診。去年10月,Grail公布的研究顯示,其陽性預測值提升至61.6%,這意味著仍有近4成陽性結果是“虛驚一場”。
批評之聲隨之而來。有學者質疑相關公司選擇性公布數據,將商業驅動的“績效指標”包裝成“變革性突破”。去年,備受矚目的NHS-Galleri試驗,結果未能在關鍵目標上達到統計顯著性。盡管公司強調在某些癌種中能顯著降低晚期診斷率,但完整的證據鏈條,仍需等待。
即便檢測能更早發現癌癥,一個更根本的問題隨之而來:相關結果是否真的能轉化為患者的生存獲益?會不會只是發現了那些惰性、易治的癌癥,而漏掉了真正致命的“元兇”?這些問題,仍有待時間給出答案。